Los fosfolípidos y el colesterol son componentes importantes de la membrana celular. Desempeñan un papel integral en el transporte transmembrana celular, la transmisión de señales y el metabolismo biológico. Pero, ¿cuáles son sus interacciones? En esta revisión de la literatura, compartiremos un artículo sobre el análisis de las interacciones entre fosfolípidos y colesterol (CHOL) mediante dos medios: dispersión y simulación de dinámica molecular. Se espera que no solo mejore nuestra comprensión de la estructura de la membrana celular, sino que también traiga inspiraciones al desarrollo de liposomas y nanopartículas lipídicas.
 Abstracto:
Abstracto:
El colesterol y los fosfolípidos son ubicuos en las membranas de las células de los mamíferos y sus interacciones son críticas en el tráfico de colesterol mediado por lípidos. Las interacciones entre el colesterol y los fosfolípidos se determinaron combinando dispersión de neutrones de ángulo pequeño (SANS), dispersión de rayos X de ángulo pequeño (SAXS) y dinámica molecular (MD) simulación de todo el átomo.
Modelado: Se construyó el modelo de distribución de densidad de dispersión de bicapas compuestas de colesterol y lípidos de éter, y se obtuvieron los parámetros estructurales de varias membranas bicapa.
Simulación: Se realizaron simulaciones de dinámica molecular con restricciones de superficie y se reprodujeron los datos experimentales. Este enfoque analítico iterativo arrojó un buen acuerdo entre las estructuras experimentales y simuladas, y las interacciones moleculares entre el colesterol y los fosfolípidos se verificaron aún más mediante simulaciones de MD.
Conclusión: · En presencia de éter lipídico, el grupo hidroxilo (-OH) del colesterol forma principalmente enlaces de hidrógeno con el grupo fosfato en la cabeza del fosfolípido. En presencia de fosfolípido, el grupo hidroxilo del colesterol forma enlaces de hidrógeno con el grupo carbonilo en la cadena de grasa fosfolípida. En Resumen, el colesterol se acerca a la superficie de la bicapa cuando hay lípidos de éter y provoca la deshidratación de los grupos fosfato en la cabeza. Además, la distribución de densidad espacial tridimensional alrededor del colesterol sugiere que se somete a un empaquetamiento anisotrópico de la cadena, lo que resulta en la inclinación del colesterol.
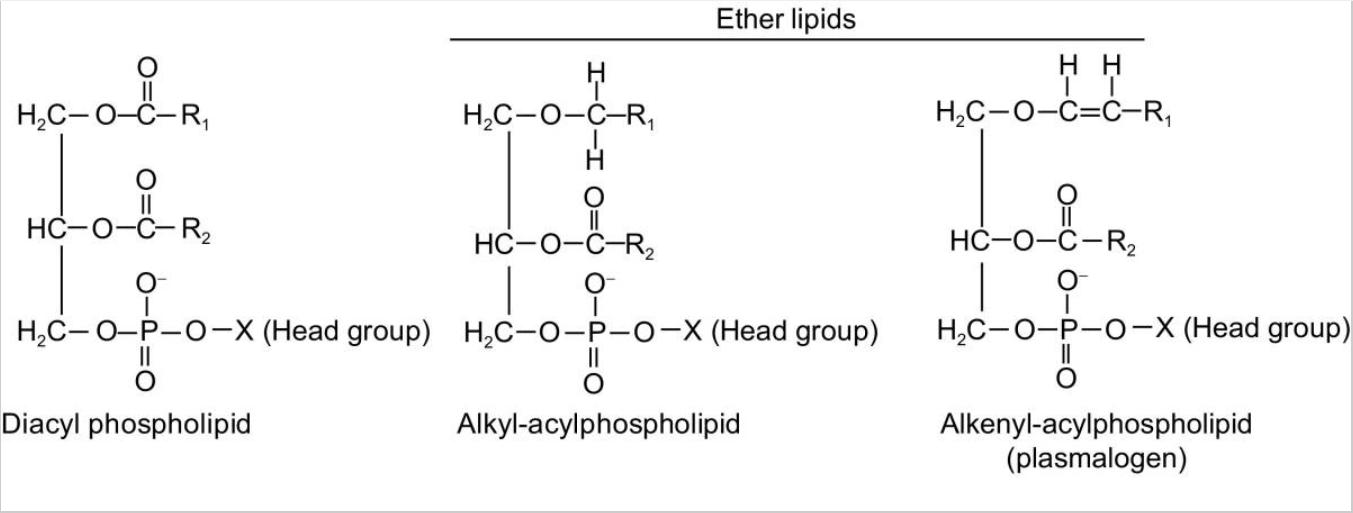
Figura 1. Estructuras moleculares de fosfolípidos y lípidos éter
Material:
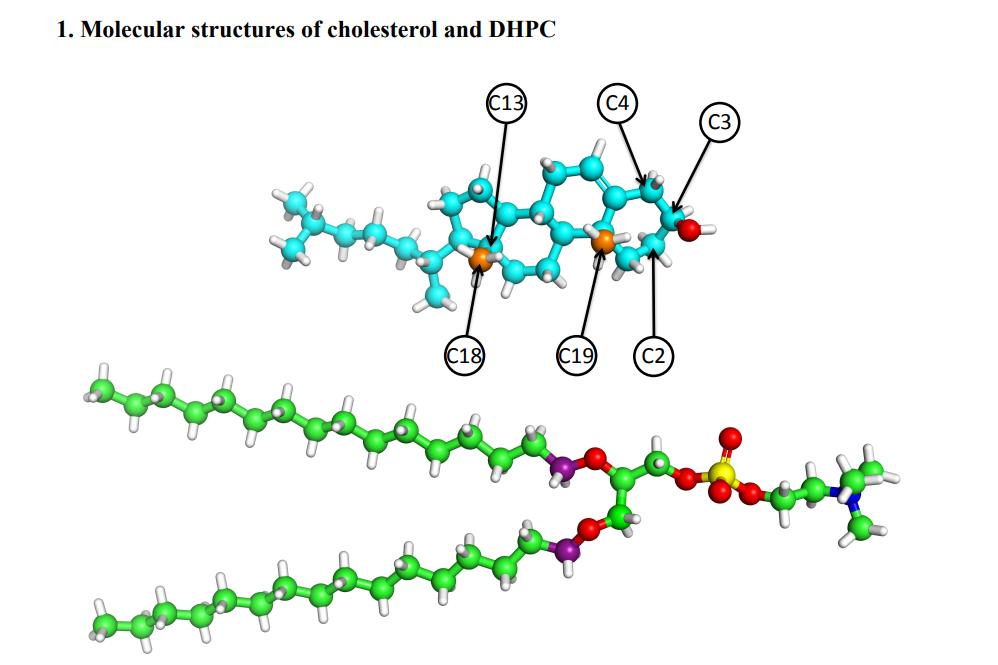
Figura 2. Estructuras moleculares de cheolesterol (CHOL) y dihexadecilfosfatidilcolina (DHPC)
El modelo construido es una bicapa lipídica compuesta de colesterol (CHOL) y dihexadecilfosfatidilcolina (DHPC). Las imágenes atómicas del modelo de distribución de densidad de dispersión (SDP) se obtuvieron primero por simulación MD sin aplicar tensión superficial, luego diferentes parámetros estructurales (área lipídica, espesor de capa hidrófoba bicapa, etc.) se determinaron, y el modelo se optimizó a continuación mediante el análisis de los datos experimentales. La simulación MD se realizó sobre la tensión superficial en la etapa posterior, y las interacciones moleculares entre el colesterol y los diferentes Lípidos se analizaron más a fondo comparando los resultados de la simulación con los resultados de la prueba.
Dispersión de neutrones de ángulo pequeño (SANS):
Las pruebas de neutrones se realizaron utilizando el EQ-SANS de BL-6 de fuente de neutrones dispersos (SNS) en el Laboratorio Nacional de Oak Ridge. El vector de dispersión total Q (0,03 <Q <0,8 Å-1) Se calculó usando un detector en un rango de WaVelengths (2,5-6,0 Å), con una distancia desde el detector hasta una muestra de 2,0 m. Usando software proporcionado por SNS para corrección y reducción de ruido, se obtuvieron intensidades unidimensionales (1D) mediante análisis de datos.
Dispersión DE RAYOS X de ángulo pequeño (SAXS):
Los datos de rayos X se recopilaron DE LA G-1 Fuente de Sincrotrón de Alta Energía de Cornell. El acoplador de carga FLICAM (tamaño lineal de 71 µm, matriz de píxeles de 1.024 Í 1.024) se utilizó para detectar la dispersión de un haz incidente colimado (0,24 Í 0,24mm2) Iluminado por rayos X a una longitud de onda de 1,17 Å en muestras ULV. La distancia de la muestra al detector fue de 505,8mm. La muestra se transfirió a un tubo capilar de cuarzo de 1,5mm y se colocó en una rejilla de temperatura controlada. La relación entre la intensidad de dispersión I y el vector de dispersión Q se obtuvo restando el promedio radial del fondo de datos bidimensionales (2D). Luego se convierte en un factor de forma de rayos X usando la misma relación que los neutrones.
Simulación de Dinámica Molecular (MD):
CHARMM-GUI Constructor de Membranas se utilizó para generar coordenadas para una bicapa DHPC pura (128 DHPC) y una bicapa DHPC con 20% mol de colesterol (128 DHPC 32CHOL).
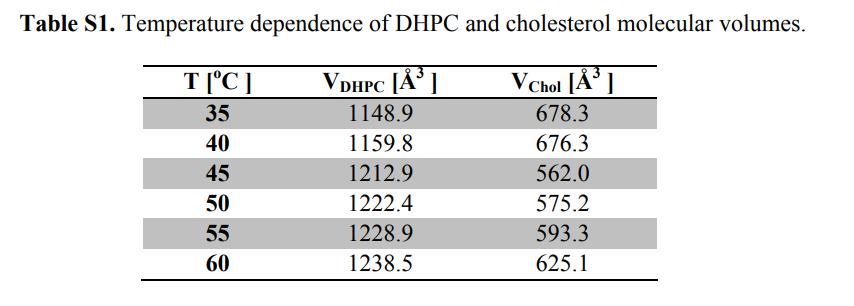
Debido a que el lípido de éter DHPC no se incluyó en la selección de lípidos de CHARMM-GUI, fue necesario construir en primer lugar el modelo de bicapa DPPC usando CHARMM-GUI, y luego cambiar el grupo carbonilo (C = O) en DPPC al grupo metileno (CH2) En DHPC. El sistema se solvató agregando moléculas de agua de 4.300 4.800, mientras que se introdujo suficiente NaCl para el equilibrio de carga. El paquete NAMD (versión 2.816) y el campo de fuerza lipídica CHARMM 36 se utilizaron para simulaciones MD. Para la optimización de campo de fuerza específica y la configuración de parámetros MD, consulte el texto original y los documentos de respaldo.
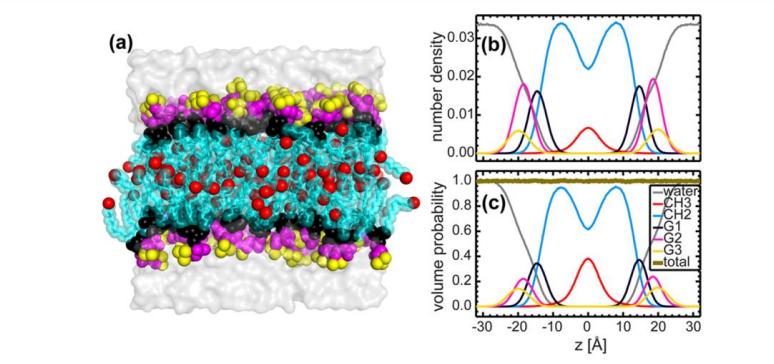
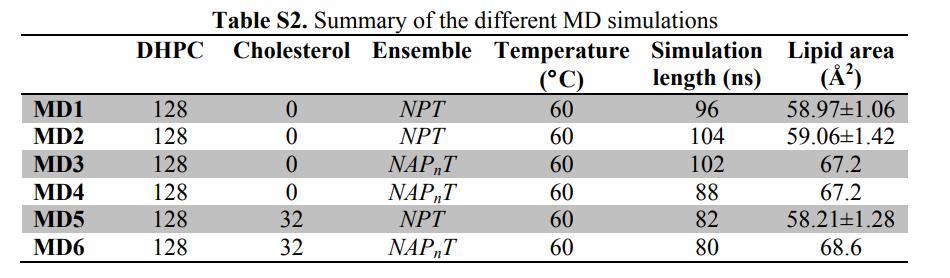
Figura 3. Sistema de simulación MD y construcción del sistema bicapa DHPC
(A) Sistemas bicapa equilibrados en los que se resuelve la bicapa lipídica en cinco componentes (diferenciación de color): rojo-metilo (CH3); Columna vertebral de glicerol negro + enlace de éter; azul claro-metileno (CH2); Grupo de cabeza púrpura (radical fosfato + CH2CH2N); y trimetil terminal amarillo-Colina.
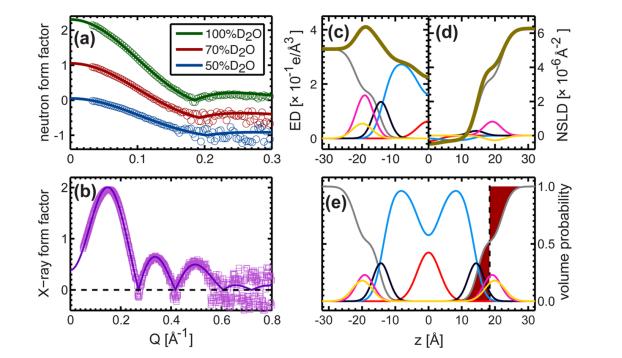
Figura 4. Elucidación de modelos de SDP por diferentes factores experimentales comparativos
(La Composición lipídica se describe por funciones analíticas (es decir, Función gaussiana y función de error), y el contenido de agua se determina mediante la complementación con la integral total del liposoma. A: dispersión de neutrones; B: dispersión de rayos X; C: densidad total de electrones; D: densidad de longitud de dispersión de neutrones; e: distribución de volumen. Nota: La Descripción del color es consistente con la figura 3)
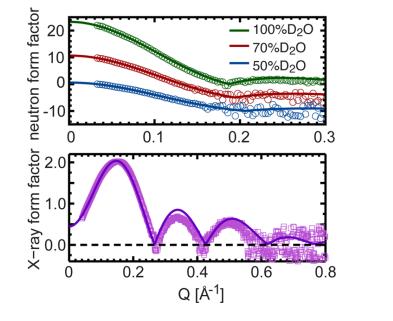
Figura 4. Comparación directa entre los factores de forma de neutrones y rayos X para diferentes experimentos de contraste
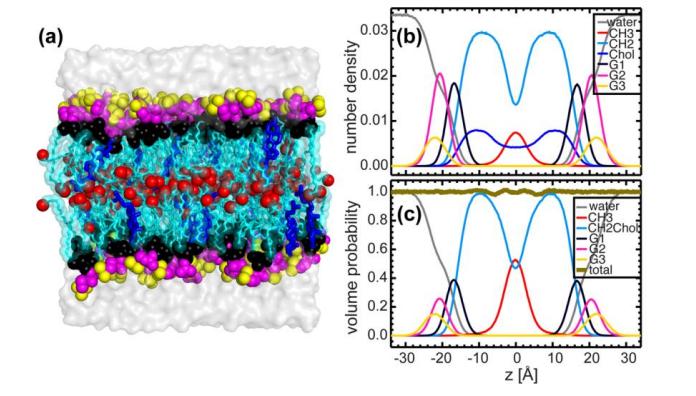
Figura 5. Simulación MD DE UNA bicapa que contiene 20% en moles de colesterol y DHPC
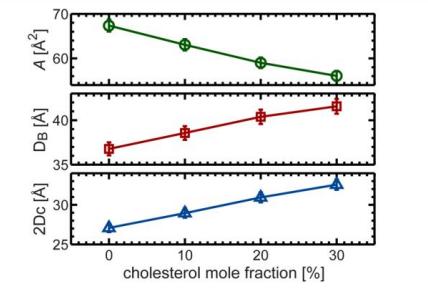
Figura 6. Concentración de colesterol frente a cambios en parámetros estructurales representativos para bicapas DHPC
(El efecto de ordenación del colesterol se demuestra por una disminución en el área lipídica de la superficie con el aumento de la concentración de colesterol, un aumento en el espesor de la membrana bicapa lipídica DBY espesor de hidrocarburos 2DC, Y un cambio aproximadamente lineal en el efecto de agregación del colesterol).
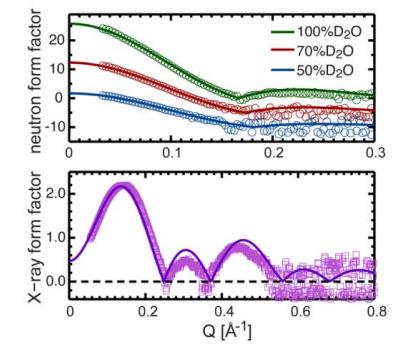
Figura 7. Comparación directa entre diferentes factores de forma experimentales para las membranas bicapa de DHPC que consisten en un 20% en moles de colesterol y factores de forma calculados por la simulación cinética de NAPnT en el área celular unitaria fija
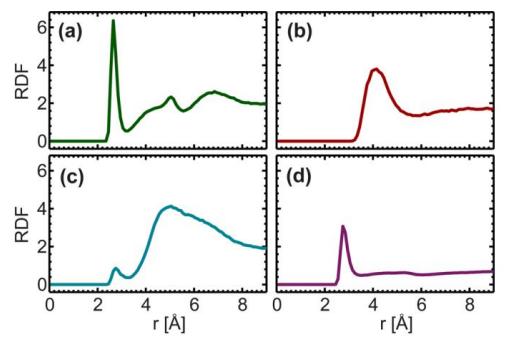
La Fig. 8. Función de distribución radial del grupo hidroxilo (-OH) del colesterol con radical fosfato (a), átomo N de colina (B), Grupo Éter de cadena principal (-O-, c), Y átomo de oxígeno en agua libre (se observó un pico agudo para el radical fosfato y el agua a 2,7 Å, Y se observó un pico amplio para el átomo de N en colina a 4 Å.)
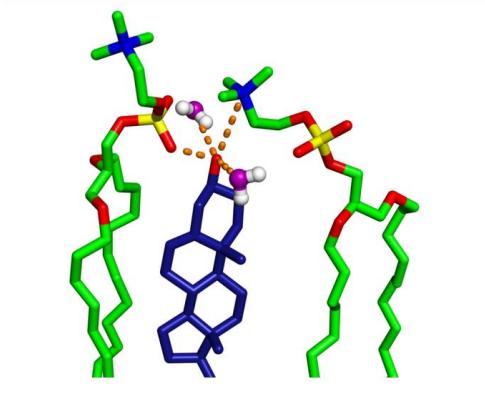
Figura 9: enlaces de hidrógeno entre los lípidos CHOL-OH y cercanos basados en la distribución de RDF en la figura 8 (el naranja indica enlaces de hidrógeno potenciales e interacciones electrostáticas).
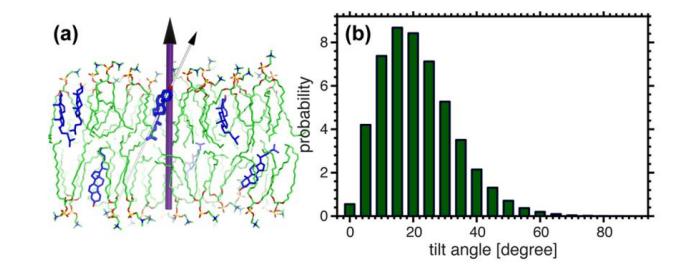
Figura 10 Obligación del tetralopo plano de colesterol con respecto al normal de la bicapa. El colesterol no se distribuye verticalmente en la membrana, sino con un cierto ángulo. La gran mayoría del colesterol tiene una distribución de inclinación de 20 °.
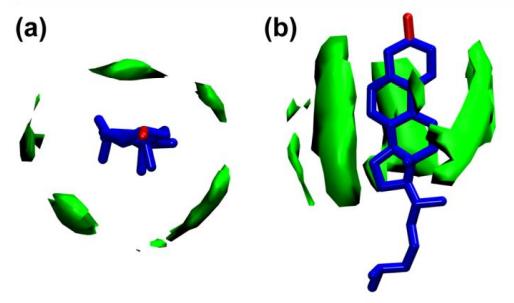
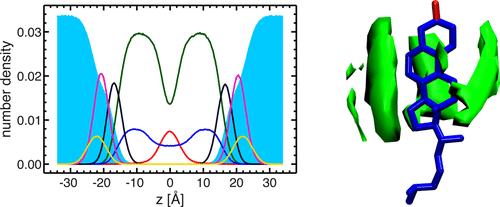
La Figura 11. Distribución de densidad 3D de cadenas de hidrocarburos alifáticos cerca del colesterol. El empaque de la cadena anisotrópica está asociado con los tetraloops de colesterol, y el empaque de la cadena de alta densidad también ocurre cerca de la cara lisa del anillo.
Conclusión:
Este estudio combinó experimentos con simulaciones. SANS y SAXS se utilizaron para investigar la posición molecular y la orientación del colesterol en bicapas lipídicas de éter. Las causas de las diferentes propiedades de dispersión de las bicapas se analizaron más a fondo mediante simulaciones MD, que formaron la base del modelo SDP para analizar los datos experimentales. Por el contrario, los parámetros del modelo se optimizaron aún más utilizando los parámetros estructurales obtenidos experimentalmente para mejorar la autenticidad y fiabilidad de las simulaciones MD y determinar las interacciones moleculares entre el colesterol y los lípidos éter. Las interacciones moleculares entre los acilfosfolípidos ordinarios y el colesterol son otra muy distinta.
Específicamente:
En las bicapas compuestas por lípidos éter, el grupo hidroxilo (-OH) sobre el colesterol forma enlaces de hidrógeno con el oxígeno en los grupos fosfato, mientras que en los fosfolípidos ordinarios, los grupos hidroxilo tienden a formar enlaces de hidrógeno con grupos carbonilo (C = O) en grasas fosfolípidas debido aPresencia de grupos éster. Esta diferencia en las interacciones puede explicar el importante papel que juegan los fosfolípidos acetales (lípidos éter) en la mediación del transporte de colesterol. Más importante aún, en el presente estudio, las interacciones entre diferentes moléculas en el entorno de la membrana se modularon aún más cambiando la composición química de los lípidos.
Colesterol, incluyendoColesterol HP, Juega un gran papel en los organismos y también es un excipiente farmacéutico importante. AVT suministra colesterol derivado de la planta. Póngase en contacto con nosotros para más información.
Referencias:
[1]. Dean JM, Lodhi IJ.Funciones estructurales y funcionales de los lípidos éter.Célula de proteína. 2018;9(2):196-206. doi: 10,1007/s13238-017-0423-5
[2]. Pan J, Cheng X, Heberle FA, Mostofian B, Kučerka N, Drazba P, Katsaras J. Interacciones entre los fosfolípidos éter y el colesterol según se determina por dispersión y simulaciones de dinámica molecular. J Phys Chem B. 2012 27 de diciembre; 116(51):14829. Doi: 10,1021/jp310345j. Epub 2012 13 de diciembre. PMID: 23199292; PMCID: PMC3539752.